Enzimas
definição
As enzimas são substâncias químicas que podem ser encontradas em todo o corpo. Eles colocam reações químicas em movimento no corpo.
história
A palavra enzima foi feito por Wilhelm Friedrich Kühne 1878 e é derivado da palavra grega inventada enzima, que significa fermento ou massa fermentada. Isso então encontrou seu caminho para a ciência internacional. O união internacional de química aplicada pura (IUPAC) e o união internacional da bioquímica (IUBMB) trabalharam juntos para desenvolver uma nomenclatura para as enzimas que define os representantes desse grande grupo de substâncias como um grupo comum. A nomenclatura, que classifica as enzimas de acordo com suas tarefas, é importante para determinar as tarefas de cada enzima.
Ilustração de enzimas
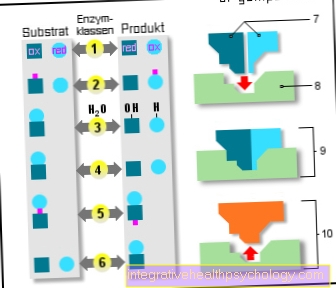
Enzimas
6 classes de enzimas:
- Oxidorredutases
(Redução de oxidação) - Transferases
(Transmissão) - Hidrolases
(Uso de água) - Lyases
(Decote) - Isomerases
(mesma fórmula empírica) - Ligases
(Reações de adição) - Substratos
- Centro ativo
- Enzima / substrato
complexo - Enzima / produto
complexo
Uma visão geral de todoss imagens do Dr. podem ser encontradas em: ilustrações médicas
Nomeação
O Nomeação a enzima está ligada três princípios básicos Sediada. Os nomes das enzimas que terminam em –ase descrevem várias enzimas em um sistema. O próprio nome da enzima descreve a reação que a enzima desencadeia (catalizado) O nome da enzima também é uma classificação da enzima. Além disso, um sistema de código que Sistema numérico CE, em que as enzimas são feitas sob um código numérico quatro números pode ser encontrado. O primeiro número indica a classe da enzima. Listas de todas as enzimas detectadas garantem que o código de enzima especificado possa ser encontrado mais rapidamente. Embora os códigos sejam baseados nas propriedades da reação que a enzima catalisa, na prática, os códigos numéricos são difíceis de controlar. Nomes sistemáticos com base nas regras acima são usados com mais frequência. Surgem problemas de nomenclatura, por exemplo, com enzimas que catalisam várias reações. Portanto, às vezes há vários nomes para eles. Algumas enzimas têm nomes triviais que não indicam que a substância mencionada seja uma enzima. Como os nomes são tradicionalmente amplamente usados, alguns deles foram mantidos.
Classificação de acordo com a função enzimática
De acordo com a IUPAC e a IUBMB, as enzimas são divididas em seis classes de enzimas de acordo com a reação que desencadeiam:
- Oxidorredutases
As oxidorredutases colocam as reações redox em movimento. Nessa reação química, os elétrons são transferidos de um parceiro de reação para o outro. Uma substância libera elétrons (oxidação) e outra substância aceita elétrons (redução).
A fórmula para a reação catalisada é A ?? + B? A? + B?.
A substância A libera um elétron (?) E é oxidada, enquanto a substância B absorve esse elétron e é reduzida. É por isso que as reações redox também são chamadas de reações de redução-oxidação.
Muitas reações metabólicas são reações redox. As oxigenases transferem um ou mais átomos de oxigênio para seu substrato. - Transferases
As transferases transferem o grupo funcional de um substrato para outro. Os grupos funcionais são grupos atômicos em compostos orgânicos que determinam as propriedades da substância e o comportamento da reação em grande medida. Os compostos químicos que possuem os mesmos grupos funcionais são agrupados em classes de substâncias devido às suas propriedades semelhantes. Os grupos funcionais serão divididos conforme sejam heteroátomos ou não. Heteroátomos são todos átomos dentro de compostos orgânicos que não são nem carbono nem hidrogênio.
Por exemplo: -OH -> grupo hidroxila (álcoois) - Hidrolases
As hidrolases dividem as ligações em reações reversíveis usando água. Ésteres, ésteres, peptídeos, glicosídeos, anidridos de ácido ou ligações C-C. A reação de equilíbrio é: A-B + H2O? A-H + B-OH.
Uma enzima que pertence ao grupo das hidrolases é, por exemplo, alfa galactosidase. - Lyases
As liases, também chamadas de sintases, catalisam a clivagem de produtos complexos de substratos simples sem separar o ATP. O esquema de reação é A-B → A + B.
O ATP é adenosina trifosfato e um nucleotídeo, que consiste no trifosfato do nucleosídeo adenosina (e, como tal, um bloco de construção rico em energia do RNA do ácido nucleico). No entanto, o ATP é principalmente a forma universal de energia imediatamente disponível em todas as células e, ao mesmo tempo, um importante regulador dos processos de fornecimento de energia. Se necessário, o ATP é ressintetizado de outras reservas de energia (fosfato de creatina, glicogênio, ácidos graxos). A molécula de ATP consiste em um resíduo de adenina, o açúcar ribose e três fosfatos (? To?) Em ligações éster (?) Ou anidrido (? E?). - Isomerases
As isomerases aceleram a conversão química dos isômeros. Isomeria é a ocorrência de dois ou mais compostos químicos com exatamente os mesmos átomos (mesma fórmula empírica) e pesos moleculares, que, no entanto, diferem na conexão ou no arranjo espacial dos átomos. Os compostos correspondentes são chamados de isômeros.
Esses isômeros diferem em suas propriedades químicas e / ou físicas, e muitas vezes também em suas propriedades bioquímicas. O isomerismo ocorre principalmente com compostos orgânicos, mas também com compostos de coordenação (inorgânicos). O isomeria é dividido em diferentes áreas. - Ligases
As ligases catalisam a formação de substâncias quimicamente mais complexas do que os substratos usados, mas, ao contrário das liases, são apenas enzimaticamente eficazes com a clivagem do ATP. A formação dessas substâncias, portanto, requer energia, que é obtida por meio da divisão do ATP.
Algumas enzimas são capazes de catalisar várias reações, às vezes muito diferentes. Nesse caso, eles são atribuídos a várias classes de enzimas.
Você também pode estar interessado nestes artigos:
- Alfa-glucosidase
- Lipase
- Tripsina
Classificação de acordo com a estrutura da enzima
Quase todas as enzimas são proteínas e podem ser classificadas com base no comprimento da cadeia de proteínas:
- Monômeros
Enzimas que consistem em apenas uma cadeia de proteína - Oligômeros
Enzimas que consistem em várias cadeias de proteínas (monômeros) - Cadeias multi-enzima
Várias enzimas agregadas que cooperam e regulam umas às outras. Essas cadeias enzimáticas catalisam as etapas sucessivas do metabolismo celular.
Além disso, existem cadeias protéicas individuais que contêm várias atividades enzimáticas, chamadas de enzimas multifuncionais.
Classificação de acordo com cofatores
Outra classificação é a classificação de acordo com a consideração dos cofatores. Cofatores, coenzimas e co-substratos são nomes de várias classificações de substâncias que influenciam as reações bioquímicas por meio de sua interação com enzimas.
Moléculas orgânicas e íons (principalmente íons metálicos) são considerados.
As enzimas proteicas puras consistem exclusivamente em proteínas e o centro ativo é formado apenas por resíduos de aminoácidos e a estrutura do peptídeo. Os aminoácidos são uma classe de compostos orgânicos com pelo menos um grupo carboxi (-COOH) e um grupo amino (-NH2).
As holoenzimas consistem em um componente proteico, a apoenzima, e um cofator, uma molécula de baixo peso molecular (não uma proteína). Ambos juntos são importantes para a função da enzima.
Coenzimas
As moléculas orgânicas como co-fatores são chamadas de coenzimas. Se estiverem covalentemente ligados à apoenzima, são chamados de grupos protéticos ou co-substratos. Um grupo prostético refere-se a componentes não proteicos firmemente (principalmente covalentemente) ligados a uma proteína com efeito catalítico.
Co-substratos são nomes de várias classificações de substâncias que influenciam as reações bioquímicas por meio de sua interação com enzimas. Como biocatalisadores, as moléculas aceleram as reações nos organismos, as enzimas aceleram as reações bioquímicas. Eles reduzem a energia de ativação que deve ser superada para que a substância possa ser convertida.















.jpg)