Sarcoma de Ewing
Todas as informações fornecidas aqui são apenas de natureza geral, a terapia do tumor sempre pertence às mãos de um oncologista experiente!
Sinônimos
Sarcoma ósseo, PNET (tumor neuroectodérmico primitivo), tumor Askin, Ewing - sarcoma ósseo
Inglês: sarcoma de Ewing
definição
No qual Sarcoma de Ewing é um de Medula óssea extrovertido Tumor ósseoque pode ocorrer entre as idades de 10 e 30 anos. No entanto, afeta principalmente crianças e jovens de até 15 anos. O sarcoma de Ewing é menos comum do que isso Osteosarcoma.
O sarcoma de Ewing está localizado nos longos Ossos longos (Fêmur (Osso da coxa) e Tíbia (Shin)), bem como na pelve ou nas costelas. Em princípio, no entanto, todos os ossos do tronco e esqueleto dos membros podem ser afetados, metástases especialmente no Pulmões é possível.
frequência
A probabilidade de desenvolver sarcomas de Ewing é <1: 1.000.000. Estudos mostraram que, para cada milhão de pessoas que vivem lá, cerca de 0,6 novos pacientes desenvolvem sarcomas de Ewing a cada ano.
Comparado com o osteossarcoma (aprox. 11%) e condrossarcoma (aprox. 6%), o sarcoma de Ewing está em terceiro lugar como outro representante de tumores ósseos malignos primários. Enquanto o sarcoma de Ewing ocorre principalmente entre as idades de 10 e 30 anos, a manifestação principal foi encontrada na segunda década de vida (15 anos de idade). É, portanto, manifestado principalmente no esqueleto em crescimento, com meninos (56%) sofrendo de sarcoma de Ewing um pouco mais frequentemente do que meninas. Se você comparar os tumores ósseos malignos primários de crianças e adolescentes, o sarcoma de Ewing está em segundo lugar: Nos sarcomas ósseos infantis, a proporção dos chamados osteossarcomas é de cerca de 60%, a proporção dos sarcomas de Ewing em torno de 25% .
causas
Como já foi explicado e apresentado no contexto do sumário, a causa que é responsável pelo desenvolvimento do Sarcoma de Ewing não pode ser totalmente esclarecido. Verificou-se, no entanto, que os sarcomas de Ewing frequentemente ocorrem quando há anomalias esqueléticas familiares ou pacientes menores de um desde o nascimento Retinoblastoma (= tumor retiniano maligno ocorrendo na adolescência). A pesquisa mostrou que as células tumorais na chamada família dos sarcomas de Ewing têm uma mudança Cromossomo # 22 Exibir. Acredita-se que essa mutação esteja presente em cerca de 95% dos pacientes.
localização
As localizações mais comuns do sarcoma de Ewing podem ser encontradas nos ossos tubulares longos, especialmente na tíbia e fíbula, ou em ossos planos. No entanto, como um câncer ósseo maligno, o sarcoma de Ewing pode afetar todos os ossos. Os ossos maiores são afetados com mais frequência, os menores raramente. Se os ossos tubulares longos forem afetados, o tumor geralmente é encontrado na área da chamada diáfise, a área do eixo.
Locais preferidos:
- aproximadamente 30% do fêmur (osso da coxa)
- aprox. 12% tíbia (canela)
- aprox. 10% úmero (osso do braço)
- aproximadamente 9% da bacia
- aproximadamente 8% de fíbula (fíbula).
Por causa da metástase hematogênica grave que ocorre no início (consulte a seção seguinte), a localização nos tecidos moles também é concebível.
Localização na pelve
O sarcoma de Ewing está localizado no osso pélvico como tumor primário (local de origem do tumor) em apenas cerca de um em cada cinco casos. Com muito mais frequência, entretanto, o tumor primário está localizado em um osso tubular longo.
Os primeiros sintomas podem ser inchaço, dor e superaquecimento na região pélvica.
Localização no pé
O pé é uma localização rara em um tumor primário. É mais comum que os tumores primários da tíbia ou fíbula favoreçam uma metástase no pé.
Se houver um inchaço doloroso claro e um superaquecimento do pé, especialmente na adolescência, o sarcoma de Ewing também deve ser excluído, além da artrite juvenil. O pior não precisa ser necessariamente presumido aqui. O diagnóstico direcionado na forma de imagens pode fornecer clareza inicial sobre as causas das queixas.
metástase
Conforme mencionado acima, isso se aplica sarcoma de Ewing como metástase precoce hematogênica (= via corrente sanguínea). Portanto, as metástases também podem se estabelecer no tecido mole. Destes, principalmente é o pulmão afetados. No entanto, o esqueleto também pode ser afetado por metástases através da corrente sanguínea.
O fato de o sarcoma de Ewing ser classificado como metastático precoce foi comprovado por estudos que mostram que as metástases podem ser detectadas em cerca de 25% dos casos no momento do diagnóstico. Como as metástases infelizmente nem sempre podem ser descobertas, a taxa de escuridão provavelmente será muito maior.
diagnóstico
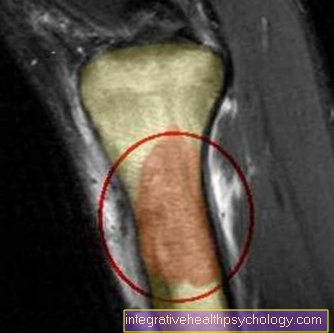
Os sarcomas de Ewing podem causar uma variedade de sintomas. Eles devem ser listados abaixo:
- Dor de causa desconhecida
- Inchaço e geralmente dor na (s) região (ões) afetada (s)
- Inchaço dos gânglios linfáticos
- sinais locais de inflamação (vermelhidão, inchaço, superaquecimento)
- perda de peso indesejada
- Restrições funcionais até paralisia
- Fratura sem evento de acidente
- Suor noturno
- leucocitose moderada (= aumento no número de leucócitos no sangue)
- desempenho diminuído
Um tumor pode ser descartado com probabilidade suficiente se os seguintes critérios forem atendidos de acordo com os diagnósticos clínicos, de imagem e laboratoriais:
- Não há evidência de uma massa
ou
O inchaço visível, a massa comprovada ou queixas pouco claras podem ser claramente explicados e documentados por uma doença não tumoral.
Diagnósticos básicos:
Em princípio, os métodos de imagem são usados para diagnósticos básicos. esses são
Exame de raio x
Exame de raios-X na área de localização do tumor (pelo menos 2 níveis)
Sonografia
Ultrassonografia do tumor (especialmente se houver suspeita de tumor de tecido mole no diagnóstico diferencial)
Para obter informações adicionais e permitir delimitações de diagnóstico diferencial, diagnósticos laboratoriais (exame de valores laboratoriais) são usados. Os seguintes valores são determinados como parte deste diagnóstico de laboratório:
- Hemograma
- Ferro (porque diminuiu em tumores)
- Eletrólitos (para descartar hipercalcemia)
- ESR (taxa de sedimentação)
- CRP (proteína C reativa)
- fosfatase alcalina (aP)
- osso específico (AP)
- Fosfatase ácida (sP)
- Antígeno específico da próstata (PSA)
- Ácido úrico (HRS): aumentado com alta renovação celular, por ex. em hemoblastose
- Proteína total: diminuída nos processos de consumo
Eletroforese de proteínas - Estado da urina: paraproteínas - evidência de mieloma (plasmacitoma)
- Marcador de tumor NSE = enolase específica de neurônio no sarcoma de Ewing
Diagnóstico especial de tumor
Imagem de ressonância magnética (MRI)
Além dos métodos de imagem mencionados no contexto do diagnóstico básico, a tomografia por ressonância magnética representa mais uma possibilidade que pode ser usada em casos individuais.
Usando MRI (tomografia de ressonância magnética), o tecido mole pode ser mostrado particularmente bem, em que a expansão do tumor para estruturas vizinhas (nervos, vasos) dos ossos afetados pode ser mostrado. Além disso, o volume do tumor pode ser estimado por meio de ressonância magnética (ressonância magnética) e a extensão local do tumor pode ser esclarecida.
Assim que houver suspeita de um tumor ósseo maligno, todo o osso portador do tumor deve ser fotografado para excluir metástases (assentamentos malignos).
Tomografia Computadorizada (TC):
(especialmente para mostrar estruturas ósseas duras (corticais))
Tomografia por Emissão de Pósitrons (PET)
(O valor ainda não é suficientemente válido)
Leia mais sobre o assunto: Tomografia por emissão de pósitrons
Angiografia de subtração digital (DSA) ou angiografia para visualizar os vasos tumorais
Cintilografia esquelética (cintilografia trifásica)
biopsia
Como mencionado várias vezes acima, a distinção entre sarcoma de Ewing e osteomielite, por exemplo, pode ser bastante difícil. Além do fato de os sintomas serem semelhantes, o raio X como tal nem sempre pode fornecer informações diretas. Se, após os chamados diagnósticos não invasivos descritos acima, ainda houver suspeita de tumor ou se houver incerteza sobre o tipo e a dignidade de um tumor, deve-se realizar um exame histopatológico (= exame de tecido).
Procedimentos abertos
Biópsia incisional
Como parte da chamada biópsia incisional, o tumor é parcialmente exposto cirurgicamente. Finalmente, uma amostra de tecido é coletada (se possível, osso e tecido mole). O tecido tumoral removido pode ser avaliado diretamente.
Biópsia excisional (remoção completa do tumor)
Só é considerado em casos excepcionais, por exemplo, se houver suspeita de malignidade (mudança de tumor benigno para maligno) de osteocondromas menores.
terapia
A abordagem terapêutica aqui é geralmente em vários níveis. Por um lado, o chamado plano de terapia geralmente prevê tratamento quimioterápico no pré-operatório (= quimioterapia neoadjuvante) Mesmo após a remoção cirúrgica do sarcoma de Ewing, o tratamento de acompanhamento terapêutico é fornecido por meio de radioterapia e, se necessário, quimioterapia renovada. Aqui, uma diferença para o osteossarcoma se torna perceptível: em comparação com o sarcoma de Ewing, o osteossarcoma tem uma sensibilidade à radiação mais baixa.
Objetivos da terapia:
A chamada abordagem terapêutica curativa (cura) é administrada especialmente em pacientes cujo sarcoma de Ewing é localizado e não apresenta metástases. Nesse ínterim, a chamada quimioterapia neoadjuvante em combinação com cirurgia e radioterapia abre novas oportunidades. Se o sarcoma de Ewing metastatiza fora dos pulmões (= doença tumoral generalizada; metástases extrapulmonares), a terapia geralmente tem um caráter paliativo (prolongador da vida) (ver abaixo).
Modalidades de terapia:
local:
- quimioterapia pré-operatória
- terapia cirúrgica (ressecção ampla ou radical após Enneking)
- radioterapia
Sistêmico:
quimioterapia antineoplásica
- Terapia de combinação (principalmente (= "primeira linha"): doxorrubicina, ifosfamida, Metotrexato / Leukovorin, cisplatin; na segunda linha (= "segunda linha"): etoposídeo e carboplatina)
(Os protocolos podem mudar a curto prazo)
Terapia curativa:
- quimioterapia multi-substância agressiva pré e pós-operatória
- Tratamento local na forma de ressecção cirúrgica do tumor ou radiação isolada
- Complemente a terapia com Pré-irradiação (por exemplo, no caso de tumores inoperáveis, não respondedores) ou por meio de pós-irradiação
- É importante mencionar, no contexto da terapia cirúrgica, que, não apenas devido ao desenvolvimento dos métodos cirúrgicos, intervenções que preservam as extremidades são possíveis em muitos casos. Porém, a perspectiva de cura sempre tem prioridade máxima, de modo que o foco deve ser sempre na radicalidade (= qualidade oncológica) e não na possível perda de função.
- A quimioterapia pode então ser continuada (veja acima). Fala-se então de uma chamada consolidação.
- Em pacientes com metástases pulmonares, intervenções adicionais na área dos pulmões, como a remoção parcial dos pulmões, podem ser necessárias.
Terapia paliativa (prolongamento da vida):
Pacientes com doença tumoral generalizada (= metástases extrapulmonares) devem localizar o tumor primário no tronco e / ou o tumor primário se mostrar inoperável. Nesses casos, apenas a terapia paliativa é geralmente possível. Nesses casos, o foco geralmente é a manutenção da qualidade de vida, de modo que a terapia se concentre no alívio da dor e na manutenção da função.
previsão
A ocorrência ou não de recorrências depende fortemente da extensão da metástase, da resposta à quimioterapia pré-operatória e da “natureza radical” da remoção do tumor. Atualmente, acredita-se que a sobrevida em cinco anos esteja em torno de 50%. As melhorias operacionais em particular tornaram possível melhorar a probabilidade de sobrevivência nos últimos 25 anos
A taxa de sobrevivência diminui com metástases primárias. Aqui, a taxa de sobrevivência é de cerca de 35%.
Chances de recuperação
Tal como acontece com outros cânceres, as chances de recuperação do sarcoma de Ewing devem inicialmente ser vistas como individualmente diferentes, porque as estatísticas mostram apenas as taxas médias de recuperação e sobrevivência.
As chances de recuperação aumentam se o tumor puder ser completamente removido cirurgicamente. Antes disso, a quimioterapia deve ser feita para diminuir o tumor. Depois que o tumor foi removido cirurgicamente, deve-se realizar mais quimioterapia para matar todas as células tumorais remanescentes.
Se o tumor não pode ser completamente removido cirurgicamente, as chances de recuperação são muito piores. O tratamento de acompanhamento com quimioterapia também deve ser realizado aqui.
Um tumor que não pode ser operado deve definitivamente ser irradiado.
Em geral, pode-se dizer que a perspectiva de cura do sarcoma de Ewing é menor se as metástases já estiverem presentes no momento do diagnóstico. Isso significa que o tumor se espalhou e está crescendo em outras partes do corpo também.
Taxa de sobrevivência
As taxas de sobrevivência em geral são dadas na medicina como o valor estatístico da “taxa de sobrevivência em 5 anos”. Isso indica em porcentagem quão grande é o número de sobreviventes após 5 anos em um grupo de pacientes definido. A taxa de sobrevivência relatada para o sarcoma de Ewing varia entre 40% e 60-70%. Essas amplas áreas decorrem do fato de a taxa de sobrevivência depender da infestação da respectiva região óssea. Por exemplo, se os ossos dos braços e / ou pernas são afetados, a taxa de sobrevivência de 5 anos é de 60-70%. Se os ossos pélvicos forem afetados, é 40%.
Qual é o risco de recaída?
A taxa de sobrevivência de 5 anos é em média 50%. Aqui pode-se supor que é um câncer agressivo e maligno. A taxa de sobrevivência de 5 anos diz que, em média, metade de todos os sarcomas de Ewing diagnosticados levam à morte.
No entanto, se nenhuma outra descoberta puder ser detectada após 5 anos após o tratamento bem-sucedido do sarcoma de Ewing, diz-se que o câncer está curado.
Cuidados posteriores
Recomendações:
- no ano 1 e 2:
Um exame clínico deve ser realizado a cada três meses. Como regra, uma verificação local de raios-X, testes de laboratório, uma TC do tórax e uma cintilografia esquelética de corpo inteiro realizada. Uma ressonância magnética local geralmente é feita uma vez a cada seis meses. - no ano 3 ao 5:
Um exame clínico deve ser realizado a cada seis meses. Como regra, uma verificação local de raios-X, testes de laboratório, uma TC do tórax e uma cintilografia esquelética de corpo inteiro realizada. Uma ressonância magnética local geralmente é realizada uma vez por ano. - Do 6º ano em diante, geralmente ocorre o seguinte uma vez por ano:
uma verificação de raios-X com exame laboratorial e uma tomografia computadorizada de tórax, bem como uma cintilografia esquelética de corpo inteiro e uma ressonância magnética local.
Resumo
A doença (sarcoma de Ewing) recebeu o nome da primeira descrição de James Ewing em 1921. São tumores altamente malignos que surgem de células neuroectodérmicas primitivas degeneradas (= células precursoras imaturas de células nervosas). Assim, os sarcomas de Ewing pertencem aos tumores sólidos primitivos, malignos.
Como mencionado acima, os sarcomas de Ewing afetam principalmente as áreas médias dos ossos tubulares longos e a pelve, mas uma aflição na parte superior do braço (= úmero) ou nas costelas também é concebível, de modo que aparecem paralelos com o osteossarcoma. Devido aos sinais de inflamação que os acompanham, é possível haver confusão com osteomielite.
Devido às metástases que ocorrem muito rapidamente (aproximadamente ¼ de todos os pacientes já apresentam os chamados assentamentos filhas no momento do diagnóstico), os sarcomas de Ewing também podem ser encontrados em tecidos moles, semelhantes aos rabdomiossarcomas. Os pulmões são geralmente os mais afetados por metástases.
As causas que poderiam ser responsabilizadas pelo desenvolvimento do sarcoma de Ewing ainda são desconhecidas. No entanto, atualmente presume-se que nem o componente genético (hereditariedade) nem a radioterapia já realizada podem ser responsabilizados pelo desenvolvimento. Verificou-se, no entanto, que os sarcomas de Ewing freqüentemente ocorrem quando há anormalidades esqueléticas familiares ou quando os pacientes sofrem de retinoblastoma (= tumor retinal maligno que ocorre na adolescência) desde o nascimento. A pesquisa mostrou que as células tumorais da chamada família dos sarcomas de Ewing apresentam uma alteração no cromossomo número 22. Presume-se que essa mutação (alteração genética) esteja presente em cerca de 95% de todos os pacientes.
Os sarcomas de Ewing podem causar inchaço e dor na (s) região (ões) afetada (s), que também podem estar associados a deficiências funcionais. Febre e leucocitose moderada (= aumento do número de leucócitos no sangue) também são concebíveis. Devido à possibilidade de confusão com osteomielite, por exemplo (ver acima), o diagnóstico nem sempre é fácil e, portanto, além dos procedimentos de imagem (exame de raios-X), uma biópsia (= exame de tecido de uma amostra de tecido) pode ser necessária.
A abordagem terapêutica aqui é geralmente em vários níveis. Por outro lado, o chamado plano de terapia costuma prever tratamento quimioterápico no pré-operatório (= quimioterapia neoadjuvante). Mesmo após a remoção cirúrgica do sarcoma de Ewing, o tratamento de acompanhamento terapêutico é fornecido por meio de radioterapia e, se necessário, quimioterapia renovada. Aqui, uma diferença para o osteossarcoma se torna perceptível: em comparação com o sarcoma de Ewing, o osteossarcoma tem uma sensibilidade à radiação mais baixa.
A ocorrência ou não de recorrências (crescimento de tumor renovado) depende muito da extensão da metástase, da resposta à quimioterapia pré-operatória e da "natureza radical" da remoção do tumor. Atualmente, acredita-se que a sobrevida em cinco anos esteja em torno de 50%. As melhorias operacionais em particular tornaram possível melhorar a probabilidade de sobrevivência nos últimos 25 anos